와이즈컴퍼니(주)는 빠르게 변화하는 규제 요구사항에 맞춰 고객사가 효과적으로 대응할 수 있도록 지원하고 있습니다.
이번 포스팅에서는 MDSAP 심사 과정 중 실제로 지적된 경부적합 사례를 바탕으로, 해당 사항에 대한 개선 방향과 지원 사례를 소개해드립니다.
1. MDSAP 경부적합 지적 사항
이번 심사에서 지적된 주요 경부적합 사항은 경영검토(Management Review)와 관련된 내용이었습니다.
‘경영검토 절차서’에는 필요한 요구사항이 정의되어 있었으나, 실제 경영검토 회의록에 해당 내용이 일부 누락되어 있다는 점이 문제로 지적되었습니다.
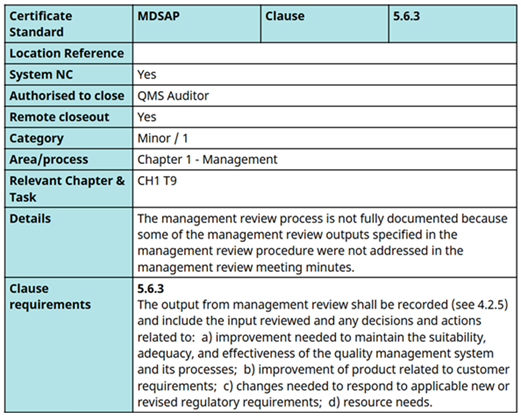
MDSAP 심사 중 지적된 경영검토 관련 경부적합 사례
경영검토는 단순한 보고 목적의 회의가 아니라, 조직의 품질경영시스템(QMS) 운영 현황을 주기적으로 점검하고 내·외부 데이터를 기반으로 문제를 분석하여 개선 방향을 결정하는 핵심 절차입니다.
여러 부서의 정보를 종합하여 경영진이 충분한 근거를 바탕으로 의사결정을 내릴 수 있도록 해야 하며, 그 과정과 결과는 반드시 문서화되어 체계적으로 관리되어야 합니다.
이렇게 기록된 경영검토 결과는 품질시스템의 지속적 개선과 조직의 품질 목표 달성에 중요한 근거 자료가 됩니다.
2. 적용되는 관련 규제 요구사항

ISO 13485:2016, Clause 5.6 – Management Review
ISO 13485의 5.6 항목은 경영검토와 관련된 요구사항을 규정하고 있으며, 그 핵심은 품질경영시스템의 적합성·적절성·효과성을 지속적으로 보장하는 데 있습니다.
MDSAP 인증을 위해서는 ISO 13485 요구사항뿐 아니라, 여러 국가의 규제 요구사항을 동시에 충족해야 하므로 각 국가별 규제 요구사항을 정확히 이해하고 반영하는 것이 필수적입니다.
국가별 경영검토 관련 규제 요구사항
- 호주 TGA – TG(MD)R Sch3 P1 1.4(5)(b)(iii)(f)
- 브라질 ANVISA – RDC 665/2022 (Art. 10, 11, 12)
- 일본 MHLW/PMDA – MO169 (Art. 18, 19, 20)
- 미국 FDA – 21 CFR 820.20(c)
공통적으로 경영검토는 계획된 주기에 따라 수행되어야 하며, 그 결과는 반드시 문서화되어야 한다는 점을 강조하고 있습니다.
특히 검토된 입력사항과 이에 따른 결정, 시정 및 예방조치, 규제 변경 대응, 고객 피드백에 따른 개선 내용이 모두 포함되어야 합니다.
이번 심사에서는 ‘경영검토 절차서’에는 ISO 13485 5.6.3 요구사항이 모두 정의되어 있었으나, 실제 회의록에 b항 및 c항(고객 피드백 기반 제품 개선 및 규제 변경 대응)이 누락되어 있다는 점이 경부적합으로 지적되었습니다.
3. 개선 방향 및 지원 내용
해당 부적합 사항에 대해 와이즈컴퍼니(주)는 다음과 같은 방향으로 개선을 지원하였습니다.
경영검토 관련 주요 지원 내용
MDSAP 요구사항과 각국 규제 요구사항을 반영한 경영검토 체크리스트를 신규 도입하였습니다.
주요 부적합 사항을 해소하기 위해 경영검토 회의록 양식을 개정하고, ISO 13485 5.6.3 및 MDSAP 요구사항에 따른 결과 요약 항목별 체크 구조를 구축하였습니다.
사전 정의된 항목에 따라 경영검토 결과가 체계적으로 기록·관리되도록 지원하였으며, 회의록 작성 이후의 후속조치 관리 절차도 함께 보완하였습니다.
경영검토의 핵심은 형식적인 회의가 아니라, 규제 요구사항을 충족하는 근거 있는 의사결정과 그 기록에 있습니다.
와이즈컴퍼니(주)는 MDSAP 규제 요구사항에 부합하는 절차와 시스템을 고객사 환경에 맞춰 맞춤형으로 지원합니다.
이를 통해 고객사는 MDSAP 단일 심사 프로그램을 통해 미국, 캐나다, 일본, 브라질, 호주 등 주요 국가의 의료기기 규제 요구사항을 효율적으로 충족할 수 있으며, 국제 규제 준수와 글로벌 시장 경쟁력 강화를 동시에 달성할 수 있습니다.