ISO 10993 생체적합성(생물학적 안전성) 시험
많은 생체적합성 시험들은 높은 비용을 들여 진행되었음에도 불구하고 시험이 ISO 10993 Series 규격에 부합하게 진행되지 않거나 보고서 내용이 이를 증명하기에 불충분하여 해외 인허가 중 규제기관에서 거절되는 일이 빈번하게 발생하고 있습니다.
와이즈컴퍼니는 이러한 불합리함을 해소하고자 미국 FDA 실사가 완료된 시험소와 협업하여 국내 대비 신속하고, 정확하고, 경쟁력 있는 비용으로 시험 서비스를 제공하고 있으며, 아래와 같은 장점이 있습니다.
첫째, ISO 17025, AAALAC, GLP 인정 기관이며, OECD GLP 및 FDA GLP (21 CFR Part 58) 기준 준수
둘째, 국내 GLP 기관 대비 낮은 시험 비용&기간
셋째, FDA/CE/MFDS 인허가 전문가의 시험 설계 & 상시 원활한 상담
넷째, 필요 시 일본 후생노동성(MHLW) 요구사항을 적용한 시험 보고서 발행
다섯째, 시험보고서는 국내(MFDS), 유럽(NB), 미국 FDA, 일본 후생노동성(MHLW) 등 규제기관에 적법하게 제출 및 활용
여섯째, ISO 10993 Series에 따른 모든 시험을 진행 가능
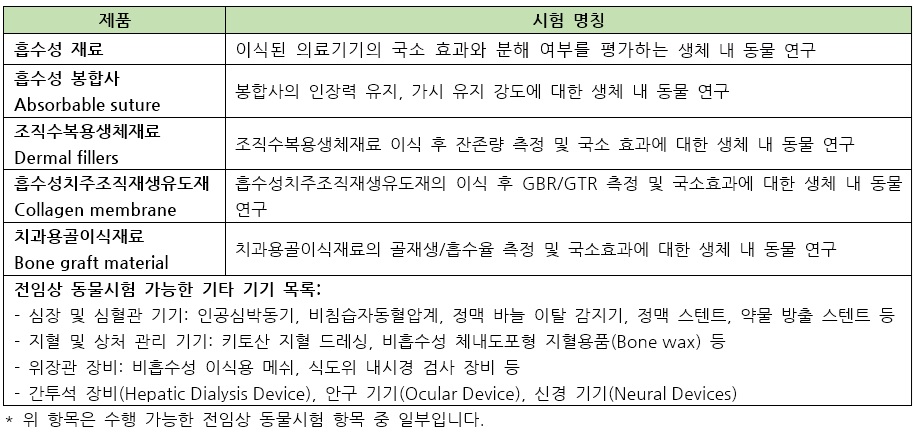
GLP 전임상 동물시험
와이즈컴퍼니는 해외 파트너 시험소와 협력하여 전임상 동물시험 서비스를 제공하고 있으며, 아래와 같은 장점이 있습니다.
첫째, 파트너 시험소는 ISO 17025 및 OECD GLP 인정 기관이며, FDA GLP (21 CFR Part 58) 기준 준수해서 시험이 수행됨.
둘째, 파트너 시험소는 30년 이상의 GLP 경험을 토대로 30만건 이상의 보고서를 해외 인허가용으로 제출된 이력이 있음.
셋째, 와이즈컴퍼니 FDA/CE/MFDS 인허가 전문가의 시험 설계 자문 & 상시 원활한 상담
일본 후생노동성(MHLW) 생체적합성(생물학적 안전성) 시험
일본 인허가를 위한 생체적합성 시험은 ISO 10993 요구사항과 일본 후생노동성(MHLW) 지침을 모두 만족하여 시험이 수행되어야 하며, 이를 준수하지 않은 시험보고서는 일본 후생노동성*MHLW)에서 반려하게 됩니다.
아래 시험들은 ISO 10993 Series 시험 방법과 다르며, 요청 시 MHLW 및 ISO 10993 Series 요구사항을 모두 준수한 생체적합성 시험이 수행됩니다. 이 시험보고서는 일본 후생노동성(MHLW)에 적법하게 제출 및 활용되고 있습니다.
세포독성, 감작성, 자극성, 물질매개발열성, 전신독성(급성, 아급성, 아만성, 만성)
시험 필요하신 시험 항목과 인허가 목적국가를 제품 정보(브로셔 혹은 사용자설명서)와 같이 이메일로 보내주시면 보다 상세한 안내 도와드리겠습니다.
생물학적 안전성 시험 관련 문의사항은 연락처의 정보로 문의 주시기 바랍니다.